在临床上常常会遇到贫血的患者,这些患者也容易出现疲劳、虚弱、头晕和呼吸困难等症状。物理治疗作为一种非药物干预手段,能够有效地改善存在功能障碍患者的症状以及生活质量。但考虑到运动尤其是高强度地运动可能影响钙的代谢或分布变化、酸中毒、氧化应激增加和脱水从而增加贫血患者的临床并发症的风险。因此,本文主要讨论贫血患者运动训练地安全性、可行性与潜在益处。
· 贫血的定义 ·
根据WHO的标准,无论病因、红细胞形态或功能如何,只要血液里的血红蛋白浓度低于对应年龄、性别和生理状态下的正常范围,即成年男性血红蛋白浓度低于130g/L、成年女性低于120g/L,即可诊断为贫血。我国标准正常值为成年男性血红蛋白不低于120g/L,非妊娠成年女性血红蛋白不低于110g/L,妊娠女性血红蛋白不低于100g/L。
贫血可由多种因素引起,主要包括:营养缺乏、饮食摄入不足或吸收障碍、感染、炎症、慢性疾病、妇产科疾病以及遗传性红细胞疾病。
1.营养缺乏是贫血的重要诱因,其中缺铁最为常见,常因膳食铁摄入不足所致。此外,维生素A、叶酸、维生素B₁₂及核黄素缺乏也可导致贫血,因为它们分别参与血红蛋白合成或红细胞生成的关键环节。其他机制还包括:因寄生虫感染、分娩或月经过多等造成的营养性失血;铁吸收障碍;新生儿铁储备不足;以及影响铁生物利用度的营养相互作用。
2.感染也是贫血的重要原因,尤其在疟疾、结核、艾滋病及各类寄生虫病高发的地区。感染可通过损害营养吸收与代谢(如疟疾、蛔虫病)或导致营养丢失(如血吸虫病、钩虫病)引发贫血。多种慢性病可诱发炎症状态,从而导致炎症性贫血/慢性病性贫血。艾滋病病毒(HIV)感染则通过红细胞无效生成或过度破坏、失血及药物副作用等多种机制致贫。
3.在妇产科方面,持续大量月经失血、妊娠期母体血容量增加,以及分娩期间和产后出血(特别是产后大出血)常导致贫血。
此外,在部分高发地区,遗传性红细胞疾病是贫血的常见原因,包括:因血红蛋白合成异常导致的α型和β型地中海贫血;因血红蛋白结构改变引起的镰状细胞病;由血红蛋白基因变异导致的其他血红蛋白病;以及红细胞酶缺陷或红细胞膜异常相关疾。
·贫血与运动训练 ·
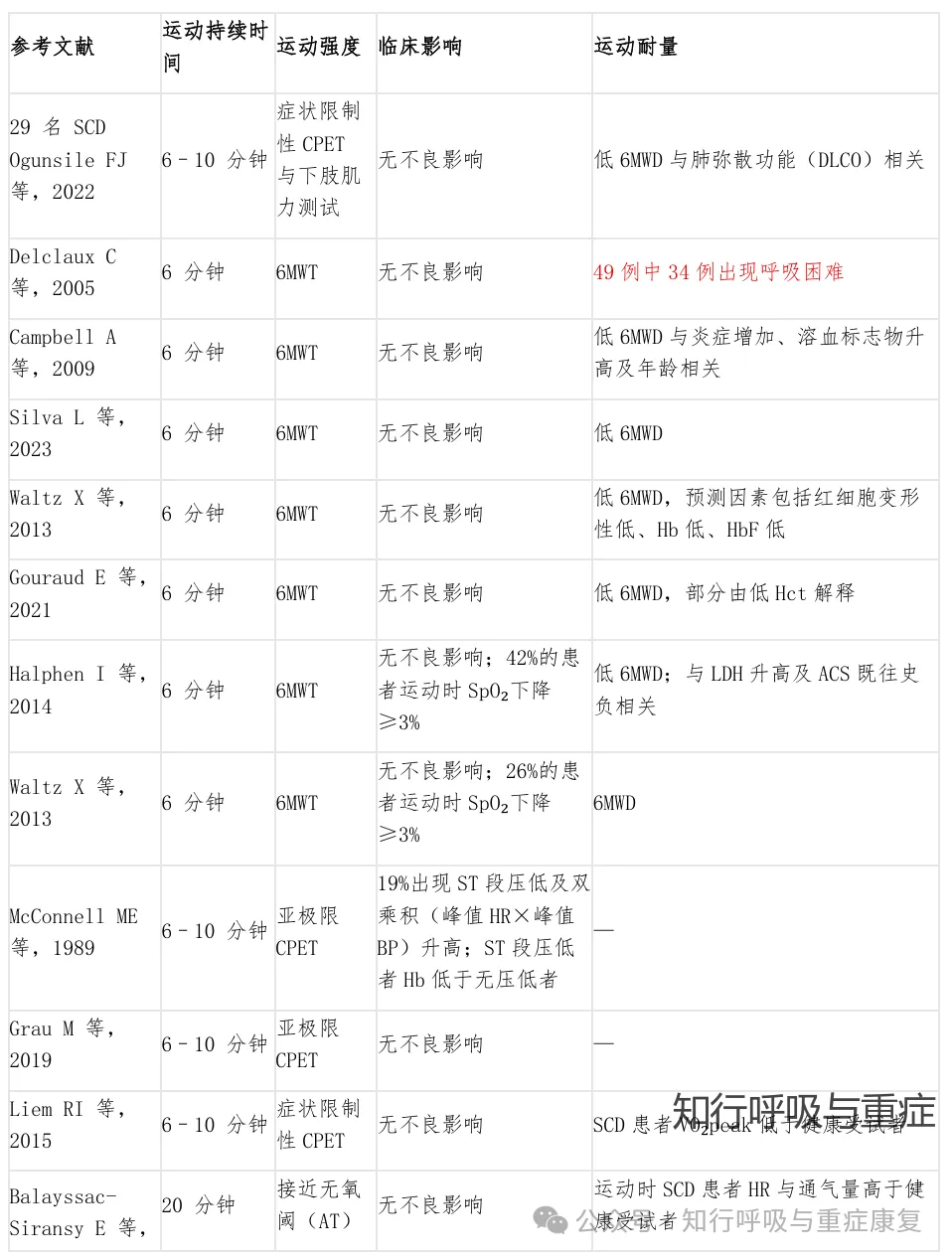
正是因为贫血发生原因复杂多样,目前贫血患者运动训练的相关安全性研究结果尚存争议,在一项关于运动训练项目对镰状细胞病(SCD)患者生理学及临床影响系统综述中,急性运动(如症状限制性心肺运动试验 CPET)总体安全,SCD患者在严密监控下进行一次性或短期的极限/次极限运动测试,不良事件发生率很低(<4%),主要包括:心电图异常占2%、需住院治疗的疼痛占0.1%、无需住院的疼痛占0.3%、运动诱发的低氧血症(即运动中血红蛋白血氧饱和度下降≥3%)占1.1%。
在接近无氧阈(AT)的 20 分钟中等强度运动中,SCD患者与对照组均未出现不良反应;数周至数月的规律中等强度耐力训练也未报告严重不良事件,反而改善了肌肉微血管结构、提高了部分心肺功能指标,且未增加疼痛危象或住院率。但运动诱发的 SpO₂下降在某些患者(尤其是儿童与青少年)中较常见(26%–42%在 6MWT 中出现 ≥3% 的下降)。因此对于此类患者,在医学监督、循序渐进、强度控制的前提下,急性运动测试和规律的中等强度训练对大多数 SCD 患者是安全且可耐受的。

但正如前文所述,贫血的原因有很多,失血、慢性疾病、化疗、骨髓癌细胞浸润、溶血或红细胞生成减少等,因此在进行运动训练前应执行严格的评估,包括有无持续性出血的存在、晕厥史、呼吸困难症状、疲劳症状,如果有条件,应进行一次心肺运动试验(CPET)。
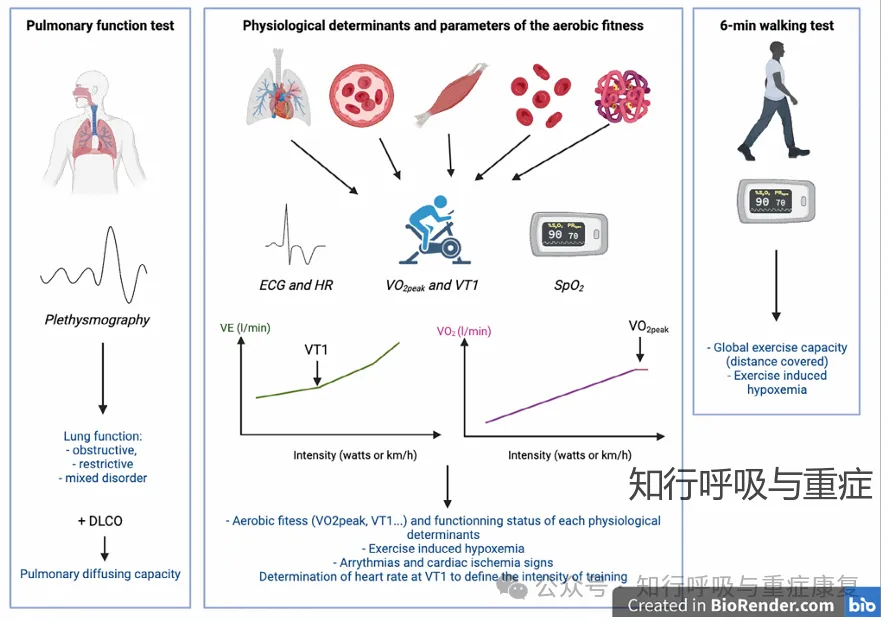
心肺运动试验(CPET)
(1)以评估患者的有氧/心肺适能水平以及体能去适应(去训练)程度;(2)峰值摄氧量(VO₂peak)、第一通气阈(VT1)及其他CPET参数可提供重要的病理生理和临床信息,包括对心肺系统、血管系统功能、肌肉功能及血氧携带能力的综合判断;(3)CPET过程中持续心电图(ECG)监测可用于发现运动诱发的心肌缺血或心律失常;(4)CPET过程中持续监测血红蛋白氧饱和度,有助于识别在运动中发生血红蛋白氧饱和度下降(即运动诱发性低氧血症)风险较高的患者;(5)通过确定VT1及其对应的心率,可帮助界定SCD患者在发生临床并发症风险较低的情况下进行运动的适宜强度。
若无法开展CPET,可采用6分钟步行试验评估患者的整体运动能力/耐量,以及在轻至中等强度运动过程中发生氧饱和度下降的风险。
对于重症患者,若无法完成CPET或6MWT,可用1分钟坐站试验或者SPPB检测患者氧饱和度下降、呼吸困难、疲劳以及低血压等风险。
Q1
贫血患者适合哪种运动方式?
目前少数针对镰状细胞病(SCD)患者训练项目效果的研究结果,骑自行车、步行、抗阻训练,以及采用徒手体操形式进行的整体拉伸与放松训练,总体上被认为是SCD患者可以安全开展的运动形式。
在另一项研究中,针对低血红蛋白的老年血液透析患者进行了为期24周抗阻训练方案,每周训练3次,每次约40分钟。训练强度采用主观用力感受量表(RPE)监测,前12周控制在RPE5–6,后12周提高至RPE 7–8。当RPE提示负荷过轻时,先增加重复次数,若超过12次则提高负荷。
Q2
运动训练方式与强度
现有针对镰状细胞病(SCD)患者(包括成人与儿童)的研究中,训练形式以有氧运动为主,通常采用功率自行车或跑步机训练。单次训练持续时间多为15–30 分钟(不包括热身与恢复阶段),每周3次。
与其他慢性疾病类似,训练前需进行一次心肺运动试验(CPET),以制定个体化训练强度。常见的强度设定方式包括:
以对应于第一通气阈(VT1)的 70% 心率或功率输出为目标;
或设定为血乳酸浓度 2.5 mmol/L 所对应的运动强度。
以最大心率的60%–75%进行步行训练
抗阻训练虽研究较少,但被证实具有可行性,建议采用相对较轻负荷,并避免或减少等长收缩,以防局部血流下降和组织缺氧。
· 运动训练能改善贫血吗? ·
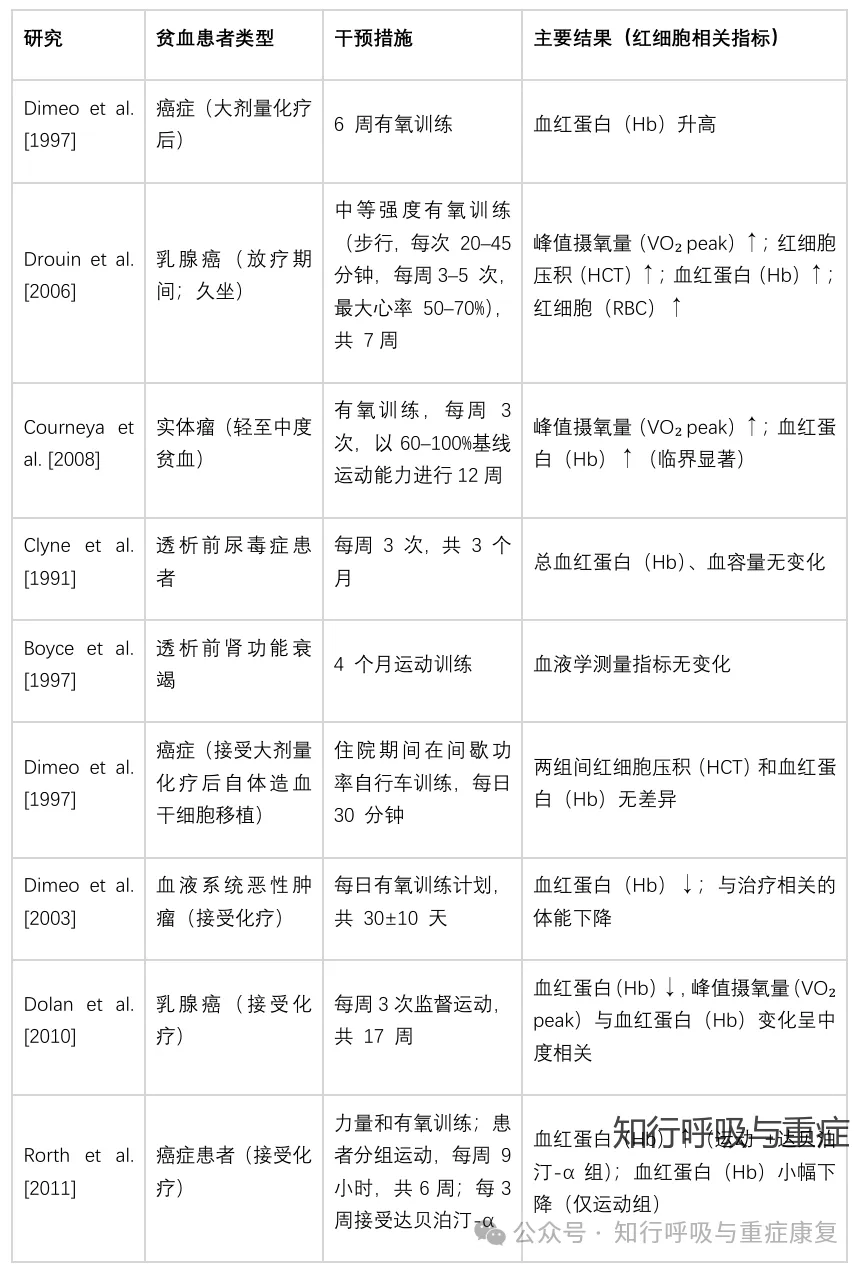
运动训练对贫血的改善效果仍有争议。部分研究显示,中等强度训练有助于缓解疾病相关贫血:如哑铃训练可改善年轻女性非贫血性缺铁;运动联合促红素治疗能减少多发性骨髓瘤患者的输血需求。次最大强度运动不影响造血因子浓度,但可提高生长激素,或与造血功能改善有关。动物实验中,长期抗阻训练比有氧训练能改善缺铁大鼠的铁状态和血红蛋白。
从目前的证据。缺氧诱导因子 HIF-1α 和 HIF-2α 在正常情况下被脯氨酰羟化酶(PHD)羟化,随后通过多泛素化途径在蛋白酶体中降解。急性运动可模拟缺氧环境,抑制 PHD 活性,使 HIF-α 稳定并转位入核,与 HIF-1β 二聚,招募转录共激活因子 p300 和 CBP,结合靶基因上的缺氧反应元件(HREs),激活 促红细胞生成素(EPO)及铁代谢相关基因。长期规律运动可提高 HIF-α 和血管内皮生长因子(VEGFα)水平,从而通过刺激红细胞生成和改善骨髓微环境,对贫血具有潜在改善作用。
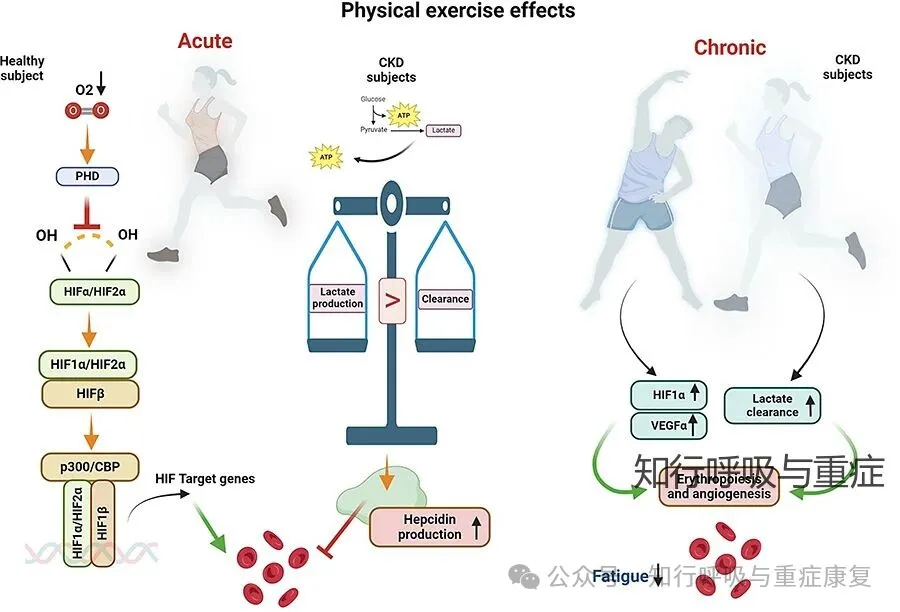
需要注意的是,急性运动可导致乳酸水平升高,在慢性肾脏病患者中,乳酸升高可短期上调肝脏铁调素表达,从而引起功能性铁受限,可能暂时抑制红细胞生成。所以运动训练时需关注乳酸的浓度。
· 总结 ·
运动训练能够刺激红细胞生成,提高总血红蛋白量及红细胞总量,从而增强机体的携氧能力。其潜在机制主要发生在骨髓,包括:促进造血骨髓增生、改善骨髓微环境、以及通过激素和细胞因子加速红细胞生成。这一适应性改变可能有助于改善贫血和提升体能。
目前运动训练被认为是一种安全、经济且有潜力的辅助改善贫血的手段。然而,不同类型贫血中运动训练的有效性,以及其最佳模式、强度和频率(尤其是力量训练),仍需进一步研究。
· 参考文献 ·
[1]Connes P, Stauffer E, Liem RI, Nader E. Exercise and training in sickle cell disease: Safety, potential benefits, and recommendations. Am J Hematol. 2024;99(10):1988-2001. doi:10.1002/ajh.27454
[2]Aucella F, Amicone M, Perez Ys ADM, et al. Does Physical Exercise Ameliorate Chronic Kidney Disease-Related Complications? The Case of Anaemia and Chronic Kidney Disease-Mineral Bone Disorder. Kidney Blood Press Res. 2024;49(1):812-820. doi:10.1159/000540659
[3]Hu M, Lin W. Effects of exercise training on red blood cell production: implications for anemia. Acta Haematol. 2012;127(3):156-164. doi:10.1159/000335620
[4]da Silva V, Corrêa H, Neves R, et al. Impact of Low Hemoglobin on Body Composition, Strength, and Redox Status of Older Hemodialysis Patients Following Resistance Training. Front Physiol. 2021;12:619054. Published 2021 Mar 10. doi:10.3389/fphys.2021.619054